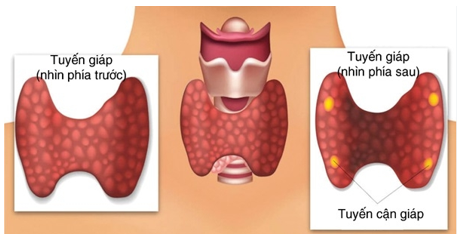
TIẾP CẬN CHẨN ĐOÁN VÀ QUẢN LÝ BỆNH NHÂN CÓ NHÂN TUYẾN GIÁP
BSNT. Vũ Thị Minh Hòa, GS. TS. Mai Trọng Khoa, PGS. TS. Phạm Cẩm Phương,
PGS. TS. Phạm Văn Thái,
Trung tâm Y học hạt nhân và Ung bướu – Bệnh viện Bạch Mai
(Tổng hợp)
- ĐẶT VẤN ĐỀ
Nhân tuyến giáp là một bệnh lý phổ biến trong thực hành lâm sàng, tuy nhiên tỷ lệ phát hiện được thông qua thăm khám nhìn – sờ chỉ đạt khoảng 5% ở nữ và 1% ở nam giới. Ngày nay, với sự phổ biến của siêu âm độ phân giải cao, tỷ lệ này có thể lên tới 19–68% tùy từng đối tượng nghiên cứu. Dù tỷ lệ phát hiện cao, chỉ khoảng 5–15% nhân tuyến giáp là nhân ác tính – nghĩa là đại đa số nhân tuyến giáp là lành tính và không đe dọa tính mạng.
Tại Việt Nam, ung thư tuyến giáp hiện đứng thứ 6 trong các ung thư phổ biến tại Việt Nam với khoảng 6.122 ca mới và 858 ca tử vong mỗi năm theo dữ liệu GLOBOCAN 2022. Điều đáng lo ngại không chỉ là số ca ung thư tăng lên, mà còn là thực trạng điều trị quá mức: nhiều bệnh nhân bị lạm dụng phẫu thuật hoặc dùng levothyroxine kéo dài không đúng chỉ định, gây tác hại không cần thiết trong khi bệnh hoàn toàn có thể theo dõi định kỳ.
Cách tiếp cận hiện đại không còn dựa chủ yếu vào kích thước nhân mà hướng đến phân tầng nguy cơ một cách có hệ thống: kết hợp đánh giá lâm sàng, phân loại siêu âm theo ACR TI-RADS, chỉ định chọc hút tế bào kim nhỏ (FNA) có chọn lọc, và điều trị cá thể hóa theo kết quả Bethesda. Chiến lược này đảm bảo phát hiện sớm những trường hợp thực sự cần can thiệp, đồng thời tránh được những can thiệp không cần thiết, phù hợp với xu hướng hạ bậc điều trị (de-escalation) trong các khuyến cáo gần đây trên toàn cầu, giúp bảo tồn tối đa chức năng tuyến giáp và nâng cao chất lượng cuộc sống cho người bệnh
- ĐÁNH GIÁ LÂM SÀNG BAN ĐẦU
Hỏi bệnh sử
Bước đầu tiên và nền tảng trong tiếp cận nhân tuyến giáp là khai thác kỹ bệnh sử. Cần khai thác tiền sử chiếu xạ vùng đầu cổ, tiền sử gia đình có ung thư tuyến giáp, hội chứng MEN2 hoặc các hội chứng di truyền liên quan (Cowden, FAP, Carney complex). Các triệu chứng gợi ý ác tính bao gồm: khàn tiếng, khó nuốt, khó thở, đau hoặc chèn ép vùng cổ, u to nhanh trong thời gian ngắn, hoặc phát hiện hạch cổ kèm theo. Cần lưu ý rằng đại đa số nhân tuyến giáp hoàn toàn không có triệu chứng và được phát hiện tình cờ qua siêu âm hoặc CT, MRI, PET/CT.
Khám thực thể
Khám vùng cổ cần đánh giá có hệ thống: mật độ nhân (mềm hay cứng), ranh giới (rõ hay không xác định), mức độ di động theo nhịp nuốt, kích thước ước lượng, có sờ thấy hạch cổ hay không. Nhân cứng, cố định, mới xuất hiện, hoặc kèm hạch cổ đáng ngờ là những dấu hiệu cảnh báo ác tính cần được đánh giá kỹ lưỡng hơn.
Một điểm quan trọng thường bị hiểu nhầm: kích thước nhân không tương quan tuyệt đối với nguy cơ ác tính. Nhân nhỏ dưới 1 cm cũng có nguy cơ ác tính cao gần tương đương nhân lớn hơn, và bướu đa nhân không giảm nguy cơ ung thư so với bướu đơn nhân. Do đó, mọi quyết định về chỉ định xét nghiệm tiếp theo phải dựa trên đặc điểm siêu âm và phân tầng nguy cơ, không phải kích thước hay số lượng nhân.
- XÉT NGHIỆM CẬN LÂM SÀNG
TSH và các xét nghiệm chức năng tuyến giáp
Định lượng TSH huyết thanh là xét nghiệm bắt buộc đầu tiên với mọi bệnh nhân có nhân tuyến giáp, kết quả TSH sẽ định hướng toàn bộ chiến lược thăm dò tiếp theo. Khi TSH giảm gợi ý cường giáp, bước tiếp theo là xạ hình tuyến giáp để xác định xem nhân có phải là nhân “nóng” (tăng hoạt động chức năng) hay không. Nhân “nóng” có nguy cơ ác tính dưới 1–3% và thường không cần chọc hút tế bào.
Khi TSH bình thường hoặc tăng, tiến hành siêu âm tuyến giáp và cân nhắc chọc hút tế bào (FNA) theo phân loại TI-RADS. Với TSH tăng gợi ý suy giáp, xét nghiệm anti-TPO giúp tìm viêm tuyến giáp Hashimoto. Định lượng calcitonin không được khuyến cáo thường quy, nhưng cần thực hiện khi có tiền sử gia đình ung thư tuyến giáp thể tủy hoặc hội chứng MEN2. Giá trị calcitonin trên 100 pg/mL gợi ý mạnh ung thư thể tủy.
Siêu âm tuyến giáp và hệ thống phân loại ACR TI-RADS
Siêu âm là xét nghiệm chi phí thấp, không xâm lấn, thời gian nhanh và có giá trị cao trong đánh giá nhân tuyến giáp. Siêu âm phát hiện các nhân không sờ thấy, xác định kích thước, số lượng, đặc điểm cấu trúc và mức độ nguy cơ của từng nhân, là xét nghiệm có độ nhạy và độ đặc hiệu rất cao. Tuy nhiên, không được sử dụng siêu âm để kết luận nhân ác tính, chọc hút tế bào hoặc sinh thiết vẫn là tiêu chuẩn vàng để đánh giá.
Các đặc điểm nghi ngờ ác tính trên siêu âm bao gồm: nhân đặc giảm âm hoặc giảm âm mạnh, vi vôi hóa (microcalcification), bờ không đều hoặc có tua gai, hình dáng cao hơn rộng (taller-than-wide) trên mặt cắt ngang, dấu hiệu xâm lấn ngoài vỏ tuyến giáp, và hạch cổ nghi ngờ di căn (vôi hóa trong hạch, cấu trúc nang, tăng mạch máu ngoại vi). Ngược lại, các đặc điểm gợi ý lành tính gồm: nang thuần túy, nốt dạng bọt biển (spongiform) với hơn 50% thể tích là vi nang, halo sign (viền giảm âm bao quanh hoàn toàn), vôi hóa thô không kèm vi vôi hóa, và nhiễu ảnh đuôi sao chổi.
Hệ thống phân loại ACR TI-RADS (2017) hiện là chuẩn mực được áp dụng rộng rãi nhất, tính điểm dựa trên năm đặc điểm siêu âm: thành phần của nhân (nang thuần túy, hỗn hợp hay đặc), độ hồi âm, hình dáng (ngang hay cao hơn rộng), đường bờ (nhẵn, thùy múi hay xâm lấn), và điểm hồi âm (vi vôi hóa, vôi hóa thô hay không có). Tổng điểm xác định mức phân loại từ TR1 (lành tính) đến TR5 (nguy cơ cao), từ đó quyết định có cần FNA hay chỉ cần theo dõi siêu âm, kết hợp với ngưỡng kích thước cụ thể.
Bảng 1. Hệ thống phân loại ACR TI-RADS và ngưỡng chỉ định FNA
| Phân loại | Đặc điểm | Nguy cơ ác tính | Ngưỡng chỉ định FNA |
| TR1 – Lành tính | Nang thuần túy | 0% | Không cần FNA |
| TR2 – Không nghi ngờ | Nang phần lớn lỏng, không đặc điểm nghi ngờ | <2% | Không cần FNA |
| TR3 – Nghi ngờ thấp | Đặc đồng âm hoặc hỗn hợp, không đặc điểm nghi ngờ | 5% | FNA ≥ 2,5 cm; Theo dõi ≥ 1,5 cm |
| TR4 – Nghi ngờ trung bình | Đặc giảm âm, 1 đặc điểm nghi ngờ | 5–20% | FNA ≥ 1,5 cm; Theo dõi ≥ 1,0 cm |
| TR5 – Nghi ngờ cao | Đặc giảm âm mạnh, ≥ 2 đặc điểm nghi ngờ | >20% |
FNA ≥ 1,0 cm; Theo dõi ≥ 0,5 cm |
Nguồn: Tessler FN et al. ACR TI-RADS White Paper. J Am Coll Radiol. 2017;14(5):587–595. Nhân < 5 mm không cần FNA ngay cả khi TR5. Với bướu đa nhân, ưu tiên đánh giá nhân có điểm TI-RADS cao nhất, không phải nhân lớn nhất.
Xạ hình tuyến giáp
Xạ hình tuyến giáp bằng 99mTc-pertechnetate hoặc 123I/131I không được chỉ định thường quy cho mọi nhân tuyến giáp. Kỹ thuật này có giá trị đặc biệt khi TSH giảm để xác định chức năng của nhân: nhân nóng (tăng tập trung phóng xạ) hầu hết lành tính và không cần FNA, nhân ấm cần đánh giá thêm, còn nhân lạnh (giảm tập trung phóng xạ) có nguy cơ ác tính 5–15% cần đánh giá bằng siêu âm và FNA theo phân loại TI-RADS. Xạ hình không thay thế siêu âm và không đánh giá chính xác kích thước nhân.
- CHỌC HÚT TẾ BÀO KIM NHỎ (FNA) VÀ HỆ THỐNG BETHESDA 2023
Giá trị và cách thực hiện FNA
Chọc hút tế bào bằng kim nhỏ (Fine Needle Aspiration – FNA) là tiêu chuẩn vàng trong xác định bản chất tế bào học của nhân tuyến giáp. Đây là kỹ thuật đơn giản, ít biến chứng, chi phí thấp, độ chính xác khoảng 95% theo AACE, với độ nhạy 68–98% và độ đặc hiệu 72–100%. FNA nên được thực hiện dưới hướng dẫn siêu âm cho tất cả các trường hợp, giúp lấy mẫu từ đúng phần đặc của nhân hỗn hợp, giảm tỷ lệ mẫu không đủ chẩn đoán từ 15% xuống còn dưới 4%.
Chỉ định FNA theo ACR TI-RADS dựa trên sự kết hợp giữa mức phân loại và kích thước nhân. Nhân TR5 cần FNA khi đạt 1,0 cm, nhân TR4 khi đạt 1,5 cm, và nhân TR3 khi đạt 2,5 cm. Nhân dưới 5 mm không cần FNA ngay cả khi thuộc TR5. Khi có hạch cổ nghi ngờ, FNA hạch kết hợp định lượng thyroglobulin hoặc calcitonin trong dịch rửa (washout) giúp tăng độ chính xác chẩn đoán di căn hạch đáng kể so với siêu âm đơn thuần.
Hệ thống Bethesda 2023
Kết quả tế bào học được báo cáo theo Hệ thống Bethesda cho Tế bào học Tuyến giáp (TBSRTC) phiên bản thứ 3 năm 2023 hiện tại là hệ thống chuẩn hóa quốc tế, phân loại kết quả thành 6 danh mục với nguy cơ ác tính và hướng xử trí rõ ràng. Phiên bản 2023 cập nhật tên danh mục theo Phân loại WHO 2022, phân nhóm danh mục III thành AUS-nuclear atypia (nguy cơ cao hơn, ~20–30%) và AUS-other (nguy cơ thấp hơn, ~6–18%), bổ sung vai trò của xét nghiệm phân tử trong phân tầng nguy cơ ở danh mục III–IV.
Bảng 2. Hệ thống Bethesda 2023 – Danh mục, nguy cơ ác tính và hướng xử trí
| Danh mục | Tên gọi Bethesda 2023 | Nguy cơ ác tính | Hướng xử trí |
| I | Không chẩn đoán được (Nondiagnostic) | 5–20% | Lặp lại FNA có hướng dẫn siêu âm |
| II | Lành tính (Benign) | 2–7% | Theo dõi lâm sàng và siêu âm định kỳ |
| III | Không điển hình không rõ ý nghĩa (AUS) | 6–30%* | Lặp FNA, xét nghiệm phân tử, hoặc theo dõi |
| IV | Nghi ngờ u nang tuyến giáp (Follicular Neoplasm) | 23–34% | Xét nghiệm phân tử; cân nhắc lobectomy |
| V | Nghi ngờ ác tính (Suspicious for Malignancy) | 45–75% | Phẫu thuật: lobectomy hoặc total thyroidectomy |
| VI | Ác tính (Malignant) | 97–100% | Phẫu thuật hoặc active surveillance (PTMC <1 cm) |
*ROM = Risk of Malignancy (nguy cơ ác tính). NIFTP (Noninvasive Follicular Thyroid Neoplasm with Papillary-like nuclear features) không còn được phân loại là ung thư từ 2017, làm giảm ROM của các danh mục III–V so với phiên bản Bethesda 2009.
- HƯỚNG XỬ TRÍ NHÂN TUYẾN GIÁP
Nhân lành tính không triệu chứng (Bethesda II)
Đây là nhóm chiếm phần lớn các nhân tuyến giáp trong thực hành lâm sàng. Chiến lược cơ bản là theo dõi định kỳ, không phẫu thuật và không điều trị thuốc ức chế TSH. Liệu pháp levothyroxine (LT4) không được khuyến cáo do nguy cơ tác dụng phụ lâu dài (loãng xương, rung nhĩ) vượt qua lợi ích không đáng kể trong thu nhỏ nhân.
Siêu âm theo dõi được thực hiện sau 12–24 tháng. Nếu nhân ổn định qua hai lần siêu âm liên tiếp, chu kỳ theo dõi có thể được giãn ra hoặc ngừng theo dõi thường xuyên sau 5 năm. FNA cần được lặp lại khi nhân tăng thể tích trên 50%, khi ít nhất hai chiều tăng hơn 20% và tăng trên 2 mm mỗi năm, khi xuất hiện đặc điểm nghi ngờ mới trên siêu âm, hoặc khi có triệu chứng cơ học liên quan đến nhân.
Nhân gây cường giáp — Nhân độc
Nhân độc (nhân tự chủ chức năng) chiếm khoảng 5% bệnh nhân có nhân tuyến giáp. Điều trị triệt để có thể bằng iode phóng xạ 131I hoặc phẫu thuật, tùy từng trường hợp cụ thể. 131I đạt tỷ lệ khỏi bệnh khoảng 75%, thể tích tuyến giáp giảm trung bình 40%; tác dụng phụ chủ yếu là suy giáp, gặp ở khoảng 10% bệnh nhân trong 5 năm đầu và tăng theo thời gian. 131I chống chỉ định tuyệt đối ở phụ nữ có thai và đang cho con bú.
Với nhân độc cường giáp dưới lâm sàng (TSH thấp nhưng FT4 bình thường) hoặc bệnh nhân không thể phẫu thuật hay dùng 131I, đốt nhiệt sóng cao tần (RFA) là lựa chọn được cân nhắc, có thể cải thiện chức năng tuyến giáp và cho phép ngừng thuốc kháng giáp tổng hợp ở dưới 50% bệnh nhân. Với bướu đa nhân độc, cắt toàn bộ tuyến giáp thường là lựa chọn tốt hơn so với 131I để tránh tình trạng điều trị không đầy đủ các nhân lạnh xen lẫn.
Chỉ định phẫu thuật
Phẫu thuật được chỉ định khi FNA cho kết quả Bethesda V (nghi ngờ ác tính) hoặc VI (ác tính), khi nhân Bethesda IV với xét nghiệm phân tử dương tính, khi nhân gây triệu chứng chèn ép (khó thở, khó nuốt, khàn tiếng), khi nhân lớn trên 4 cm hoặc nang tái phát nhiều lần, khi có bướu giáp chìm, hay vì lý do thẩm mỹ. Phẫu thuật cũng được cân nhắc với Bethesda III tùy kết quả phân tử và đặc điểm lâm sàng.
Về phạm vi phẫu thuật, khi đã xác nhận ung thư tuyến giáp biệt hóa, cắt toàn bộ tuyến giáp (total thyroidectomy) là tiêu chuẩn; tuy nhiên, ATA 2025 chấp nhận cắt một thùy (lobectomy) cho ung thư nguy cơ thấp (pT1a–T2, N0, không có yếu tố nguy cơ đặc biệt). Nạo vét hạch cổ trung tâm (level VI) được thực hiện khi có hạch di căn trên lâm sàng hoặc hình ảnh. Kinh nghiệm của phẫu thuật viên đóng vai trò quyết định trong việc hạn chế tổn thương thần kinh quặt ngược và suy cận giáp vĩnh viễn.
- ĐIỀU TRỊ ÍT XÂM LẤN: RFA, TIÊM CỒN VÀ CÁC KỸ THUẬT ĐỐT NHIỆT
Đốt sóng cao tần (Radiofrequency Ablation – RFA)
RFA hiện được Hội Y học Tuyến giáp Hàn Quốc (KSThR) và Hội Tuyến giáp châu Âu (ETA 2023) khuyến cáo là lựa chọn thay thế phẫu thuật cho nhân tuyến giáp lành tính có triệu chứng hoặc ảnh hưởng thẩm mỹ. Thủ thuật được thực hiện ngoại trú, không cần gây mê toàn thân, bảo tồn hoàn toàn chức năng tuyến giáp còn lại, đây là ưu điểm vượt trội so với phẫu thuật về mặt chất lượng cuộc sống sau điều trị.
Chỉ định RFA bao gồm nhân lành tính Bethesda II gây chèn ép hoặc ảnh hưởng thẩm mỹ, nhân độc tự chủ thể tích trên 20 ml khi bệnh nhân từ chối hoặc chống chỉ định với phẫu thuật và 131I, và trong một số hướng dẫn mới nhất có thể xem xét đối với ung thư tuyến giáp thể nhú nguy cơ thấp. Kết quả điều trị cho thấy giảm thể tích nhân 50–80% sau 12 tháng, cải thiện triệu chứng rõ rệt. Tỷ lệ cần điều trị lại khoảng 10–15% sau 3 năm.
Kỹ thuật RFA đã được chứng minh tính an toàn và hiệu quả qua nhiều năm theo dõi. Ngoài RFA, các kỹ thuật đốt nhiệt khác gồm đốt laser, đốt vi sóng (MWA) và siêu âm tập trung cường độ cao (HIFU) đều có ưu và nhược điểm riêng về thời gian thủ thuật, chi phí và khả năng tiếp cận. Hiện tại dữ liệu theo dõi dài hạn đang tiếp tục được tích lũy.
Tiêm cồn tuyệt đối qua da (Percutaneous Ethanol Injection – PEI)
Tiêm cồn tuyệt đối gây hoại tử đông vón tại chỗ và tắc các mạch máu nhỏ trong nhân. Kỹ thuật này đặc biệt hiệu quả với nang tuyến giáp tái phát sau hút dịch nhiều lần, giảm trên 50% thể tích ở khoảng 90% bệnh nhân. Hiệu quả tốt nhất ở mũi tiêm đầu tiên và giảm dần với các lần tiêm sau, đặc biệt kém hiệu quả hơn với bướu đa nhân. Mỗi lần tiêm không vượt quá 10 ml. Tác dụng phụ bao gồm đau nhẹ vừa tại chỗ tiêm kéo dài 1–2 ngày, nuốt vướng, và rất hiếm liệt dây thanh âm hoặc hoại tử da.
- ĐIỀU TRỊ I-131 SAU PHẪU THUẬT UNG THƯ TUYẾN GIÁP THỂ BIỆT HÓA
Theo ATA 2025, điều trị 131I sau phẫu thuật không được khuyến cáo thường quy cho mọi bệnh nhân ung thư tuyến giáp biệt hóa mà phải dựa trên phân tầng nguy cơ tái phát. Với nhóm nguy cơ cao, 131I được khuyến cáo để điều trị ung thư tồn dư, xóa mô giáp và tăng khả năng theo dõi bằng thyroglobulin và xạ hình toàn thân. Với nhóm nguy cơ trung bình cần cân nhắc nhiều yếu tố, cá thể hóa theo từng trường hợp. Với nhóm nguy cơ thấp, bao gồm ung thư tuyến giáp thể nhú sau cắt thùy, không có chỉ định điều trị 131I thường quy.
Với ung thư tuyến giáp biệt hóa kháng iode phóng xạ (RAIR-DTC) có tiến triển toàn thân, ATA 2025 khuyến cáo điều trị bằng thuốc ức chế kinase đa mục tiêu, trong đó lenvatinib và sorafenib là lựa chọn đầu tay. Với các trường hợp có biến đổi gen đặc hiệu (NTRK, RET, ALK, BRAF V600E), thuốc nhắm trúng đích tương ứng được ưu tiên do hiệu quả cao hơn và độc tính chọn lọc hơn.
- THEO DÕI LÂU DÀI VÀ CHIẾN LƯỢC HẠ BẬC
Theo dõi nhân lành tính
Với nhân lành tính ổn định, siêu âm theo dõi được thực hiện sau 12–24 tháng. Nếu nhân không thay đổi qua hai lần siêu âm liên tiếp, ETA 2023 cho phép giãn chu kỳ theo dõi lên 3–5 năm. FNA lặp lại được chỉ định khi nhân tăng kích thước có ý nghĩa, xuất hiện đặc điểm siêu âm nghi ngờ mới, hoặc có triệu chứng cơ học.
Theo dõi sau điều trị ung thư tuyến giáp biệt hóa
ATA 2025 nhấn mạnh khái niệm Dynamic Risk Stratification — đánh giá lại nguy cơ theo thời gian dựa trên đáp ứng điều trị, thay vì áp dụng cùng một cường độ theo dõi cho tất cả bệnh nhân. Bốn mức đáp ứng được xác định: đáp ứng tốt (Excellent Response), đáp ứng về sinh hóa không hoàn toàn, đáp ứng về cấu trúc không hoàn toàn, và đáp ứng không xác định, mỗi mức tương ứng với chiến lược theo dõi và quyết định điều trị khác nhau.
Siêu âm vùng cổ kết hợp định lượng thyroglobulin (Tg) và anti-Tg được thực hiện mỗi 6–12 tháng trong hai đến ba năm đầu sau điều trị, sau đó hàng năm nếu tình trạng ổn định. Với bệnh nhân có đáp ứng tốt và nguy cơ thấp, ATA 2025 cho phép giảm cường độ theo dõi hoặc ngừng theo dõi sinh hóa sau 5–10 năm, đây là một thay đổi quan trọng so với ATA 2015 nhằm giảm gánh nặng y tế và lo lắng không cần thiết cho bệnh nhân.
Theo dõi tích cực thay thế phẫu thuật (Active Surveillance)
Active surveillance (theo dõi tích cực thay vì can thiệp ngay) được ATA 2025 khuyến cáo như một lựa chọn khả dĩ cho ung thư tuyến giáp thể nhú dưới 1 cm không có xâm lấn, không có di căn hạch hay di căn xa. Phương án này đặc biệt phù hợp với bệnh nhân cao tuổi, có bệnh lý nền nặng hoặc bệnh nhân không muốn phẫu thuật sau khi được tư vấn đầy đủ. Siêu âm được thực hiện mỗi 6–12 tháng trong năm đầu, sau đó mỗi 12–24 tháng. Quyết định chuyển sang phẫu thuật khi nhân tăng kích thước, xuất hiện hạch, hoặc theo nguyện vọng của bệnh nhân.
- KẾT LUẬN
Tiếp cận nhân tuyến giáp ngày nay là một chiến lược đa tầng, dựa trên bằng chứng và hướng đến cá thể hóa điều trị. Trung tâm của chiến lược này là siêu âm ACR TI-RADS kết hợp FNA chọn lọc theo Bethesda 2023, đặt trong bối cảnh đánh giá lâm sàng toàn diện. Xạ hình tuyến giáp, xét nghiệm phân tử, RFA và 131I đều có vai trò cụ thể trong từng nhóm bệnh nhân, không thể áp dụng đồng loạt.
Thông điệp cốt lõi của ATA 2025 và ETA 2023 là hạ bậc điều trị (de-escalation) có kiểm soát: phát hiện sớm và điều trị triệt để những trường hợp ung thư thực sự cần can thiệp, đồng thời tránh phẫu thuật, điều trị 131I và theo dõi quá mức cho nhóm nguy cơ thấp vốn có tiên lượng rất tốt ngay cả khi chỉ theo dõi định kỳ. Tại Việt Nam, với tỷ lệ nhân tuyến giáp cao và xu hướng điều trị quá mức còn phổ biến, việc áp dụng nhất quán TI-RADS, Bethesda và các hướng dẫn ATA/ETA cập nhật là bước đi cần thiết nhằm hạn chế điều trị quá mức để nâng cao chất lượng chẩn đoán và điều trị cho bệnh nhân.
TÀI LIỆU THAM KHẢO
- Haugen BR, Alexander EK, Bible KC, et al. 2015 American Thyroid Association Management Guidelines for Adult Patients with Thyroid Nodules and Differentiated Thyroid Cancer. Thyroid. 2016;26(1):1–133.
- Ringel MD, et al. 2025 American Thyroid Association Management Guidelines for Adult Patients with Differentiated Thyroid Cancer. Thyroid. 2025;35(8):841–985.
- Tessler FN, Middleton WD, Grant EG, et al. ACR Thyroid Imaging, Reporting and Data System (TI-RADS): White Paper of the ACR TI-RADS Committee. J Am Coll Radiol. 2017;14(5):587–595.
- Cibas ES, Ali SZ. The 2023 Bethesda System for Reporting Thyroid Cytopathology. Thyroid. 2023;33(10):1039–1044.
- Leenhardt L, Erdogan MF, Hegedüs L, et al. 2023 European Thyroid Association Clinical Practice Guidelines for Thyroid Nodule Management. Eur Thyroid J. 2023;12(5):e230067.
- Tran NQ, Le BH, Hoang CK, et al. Prevalence of Thyroid Nodules and Associated Clinical Characteristics. Risk Manag Healthc Policy. 2023;16:899–907.
- Sung H, Ferlay J, Siegel RL, et al. Global Cancer Statistics 2022: GLOBOCAN Estimates. CA Cancer J Clin. 2024;74(3):229–263.
- Nguyen BQ, Tran HT, Nguyen HTT, et al. Clinical, cytological and ultrasonographic features of incidental thyroid cancer in Vietnam. Endocrinol Diabetes Metab. 2023;6(3):e415.
- Kim JH, Baek JH, Lim HK, et al. 2017 Thyroid Radiofrequency Ablation Guideline: Korean Society of Thyroid Radiology. Korean J Radiol. 2018;19(4):632–655.
- Vu DL, Le TM, et al. Efficacy and Safety of Radiofrequency Ablation for Autonomously Functioning Thyroid Nodules. Ther Clin Risk Manag. 2022;18:11–19.
- Le THV, Pham KL, Nguyen PBQ. Research value of ultrasonographic and TIRADS 2017 classification as ACR. Vietnamese Journal of Radiology and Nuclear Medicine. 2018;29:81–86.
- Uludag M, Unlu MT, Isik C, et al. What Has Changed in the 2025 ATA Guidelines? Sislietfaltip. 2025;59(3):263–272.